最終更新日が2023年以前の記事です。レイアウト変更のため、正常に表示されない場合があります。
最近ちょっと久々に気になって、共通試験の化学の問題を覗き見してみたのですが……
あるトリグリセリドX(分子量882)の構造を調べることにした。Xを触媒とともに水素と完全に反応させると、消費された水素の量から、1分子のXには4個のC=C結合があることがわかった。また、Xを完全に加水分解したところ、……(以下略)
共通テスト 2023 化学 第4問 問4 より
……あ、新体制でもまだやるんだ、この問題。
今時誰もそんなめんどくさいことしないよ!!!
とまあ多くの化学系教育者が「いつになったらこの問題やめるんだろう」と思っていること間違いなしの有機化学分野の構造決定問題。まあ実際には有機化学をやる上での基礎的な計算能力を測るために題材として有用なのであえて残しているのではないかと思いますが(そうじゃないならほんとに消した方がいい)、「目に見えない分子の構造ってこうやって決定するんだ!」という悲しい勘違いはなくせるならその方がよっぽどいいです。
今回から数回に分けて、構造解析用の分析方法について復習がてら私の知る限りのことを色々書いてみることにしました。冒頭の話とちょっとターゲットはズレますが、薬学部の分析化学分野の講義では必ず通る道なので、参考になれば幸いです。
第1回の今回はMS(質量分析法)です。
Contents
MS(質量分析)
未知の化合物の分子量そのものを測る方法で、MS は Mass Spectrometry の頭文字です。専用の分析装置がどこの研究所にも置いてあるはずです。
数mL の試料を直接分析機器に導入するだけで、分子量はいくつです、と答えが出てきます。あら簡単。
原理(大学講義レベルの説明)
装置は試料導入部、イオン化部、質量分離部、検出部の4つに分かれています。全部まとめてコンピューターで統御されているのが普通です。
このうち重要なのはイオン化部と質量分離部。この2点にMSの動作原理が詰まっています。
イオン化部
まず、試料導入部から入った分子は、いくつかの方法でイオン化されます。代表的なのが分析対象の分子に電子をぶつけてイオン化させるEI (Electron Ionization、電子衝撃イオン化)と呼ばれる方法です。
この時、化合物の分子の質量をそのまま持った分子イオン(M+ ないし M–)が生成します。
M + e– → M・+ + 2e–
M + e– → M・–
その他、分子の構造によって結合が切れやすい部分で切れて(フラグメンテーション)、フラグメントイオンを生成します。化合物の構造によって、フラグメンテーションが起こらずほとんど分子イオンしか生成しないもの、逆に切れやすく分子イオンがほとんど観測できないものなど色々なものがあります。
- 分子イオン:化合物の質量をそのまま持ったイオン(生成するイオンの中で最も質量が大きい)。
- フラグメントイオン:同時に生成するその他(ほぼ)全てのイオン。
フラグメンテーションのパターンは化合物固有
フラグメンテーションのパターンは化合物に固有のものなので、質量分析だけで化合物の構造をある程度推定することも可能です。
例えば、メチルエチルケトン(2-ブタノン)のスペクトルはこんな感じですが……
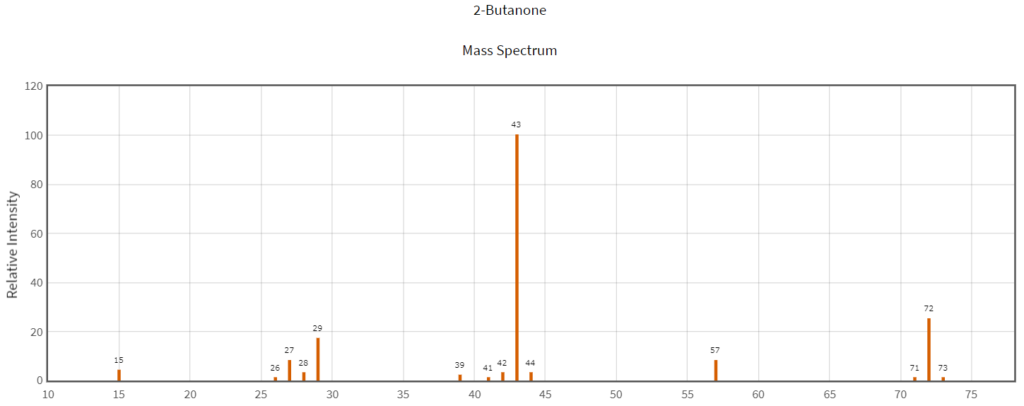
その構造異性体(分子量は同じ)であるテトラヒドロフランのスペクトルはこんな感じになります。
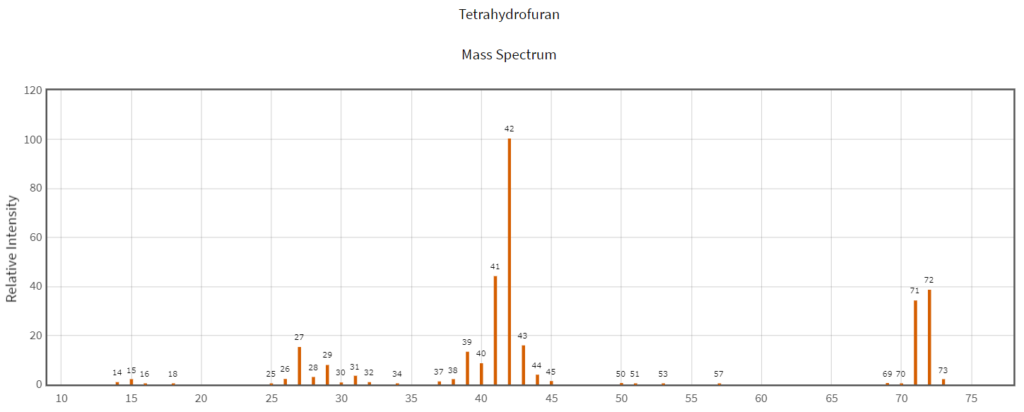
分子イオンの比率や生成しているフラグメンテーションイオンの種類が若干違いますよね。THFの方がフラグメンテーションを起こしづらいのでこのような傾向が生まれます。現実にはこの程度の分子の構造であれば、MSとって既存のライブラリと照合すれば何の分子であるかは一発です。
イオン化には他にも多数の手法がありますが、ここでは名前を挙げるにとどめます(種類こそ多いですがあまり使われていないものも多数あるので、私が実際に見たことがあるものだけ挙げています):
- CI (Chemical Ionization, 化学イオン化)
- FAB (Fast Atom Bombardment ionization, 高速原子衝撃イオン化)
- LD (Laser Desorption ionization, レーザー脱離イオン化)
- MALDI (Matrix-Assisted Laser Desorption Ionization, マトリックス支援レーザー脱離イオン化)
- ESI (ElectroSpray Ionization, エレクトロスプレーイオン化)
- などなど…
MALDI は特に高分子のイオン化に強いため、後述するTOFMSと組み合わせて使用されることが多いです。
質量分離部
帯電したイオンは高電圧に印加したスリット間に送られ、ここで加速します。レールガンでイオンを発射しようとしているようなものだと思っておけばいいです(実際この後発射されます)。
さて、この時イオンの質量が \(m\) 、電子1個当たりの電荷量が \(q\) 、イオンの電荷数が \(z\) だとします(\(z\) は通常1です)。これがスリット間にかけられた加速電圧 \(V\) で加速されて速度 \(v\) を得た時、このイオンの運動エネルギーは以下の式で表されます。
$$\frac{1}{2}mv^2=zqV$$
これは化合物の構造によらず一定であるということに留意してください。サリチル酸メチルだろうがバニリンだろうが、等しくC8H8O3であれば得る運動エネルギーは同じで、化合物の質量(∝分子量)によるというわけです。
この荷電イオンを質量分離部に打ち出し、\(m/z\) に従って分離します。分離の方法も様々な方式がありますが、まずは最も代表的な磁場型について解説します。
質量分離部にはイオンが入ってくる方向と垂直方向に磁場 \(B\) がかかっており、検出器はイオンが入ってくる方向と角度をつけて設置されています。
打ち出された荷電イオンが移動と垂直方向の磁場に入るとローレンツ力が働くため、荷電イオンは円軌道を描きます。この時、イオンにかかる遠心力と磁力は釣り合いますので、以下の式が成り立ちます。
$$\frac{mv^2}{r}=zqvB$$
これを式変形すると以下が導かれます。
$$v=\frac{rzqB}{m}$$
これを最初の式に代入して整理すると以下のようになります。
$$\frac{m}{z}=\frac{r^2q}{2V}B^2$$
さて、ここで電子1個当たりの電荷量 \(q\) は一定ですので、加速電圧 \(V\) を一定にしてやれば、磁場 \(B\) を少しずつ変えていくことで理論上はあらゆる \(m/z\) のイオンを検出器で捉えることが可能です。また、ある荷電イオンが磁場 \(B\) の時に検出器で検出された場合のイオンの \(m/z\) は逆算できる、ということにもなりますね。
より大きな分子の分析 – TOFMS
さて、先程の方法では磁場の変化でイオンを検出していましたが、これは測定限界が磁場の可変域によるということで、タンパク質などあまり大きな分子を測定するのにはやや不向きだということが言えそうです。そこで最近利用されているのが飛行時間型質量分析計 TOFMS (Time Of Flight Mass Spectrometer)です。「トフマス」って言ったりします。
最初の運動エネルギーの式に戻ります。
$$\frac{1}{2}mv^2=zqV$$
これをいきなり式変形しますと以下のようになります。
$$v=\sqrt{\frac{2zqV}{m}}$$
加速電圧 \(V\) で加速されたイオンは、単純にその質量 \(m\) が軽いものほど高速に飛行します。そのため、一定の距離を飛行する時間を測定、記録することで質量スペクトルを得るのが TOFMS です。ちなみにこのイオンの飛行時間は一般に \(10^{-7}\)秒以下です。
応用
MSは分離分析の手段と組み合わせることが容易です。例えば GC (Gas Chromatography, ガスクロマトグラフィー)で分離した物質の検出に MS を導入することにより、一度の分析でより多くの構造情報を得ることができます。これがいわゆる GC/MS です。
同様に LC (Liquid Chromatography, 液体クロマトグラフィー)でも同じように検出にMSを利用することができます。この場合はキャリアーとなる液体が MS による分析の邪魔になるので技術的な難易度がやや高く、GC/MS よりも実用化されたのは遅いですが、現在では普通に使われている手法です。
余談・MS の思い出話
MS は私が大学の研究室に所属している間はずっとお世話になった装置でした。有機化学や医薬品化学、生薬学など低分子化合物を扱う研究室では必ず、他にももしかするとタンパク質を扱う研究室でもヘビーユーザーになるかもしれません。私は天然物由来の化合物とその誘導体の構造決定をしていたので、抽出してMSで分析して分子量特定+NMR(次回扱います)で構造決定、みたいなのがよくありました。
分析にそれほどお金も時間も要らないため重宝されていましたが、時々誰かが汚いサンプルを打ったりなんかするとその後のスペクトルがしばらく乱れっぱなしになるので、「誰だこんなきたねえサンプル打ったのはこらぁ(怒)」みたいな話をよくしてました。まあ汚いサンプルを打っちゃいけないのはどの分析機器でも同じなのですが、MSは結構汚染に弱いのでこれから使う皆さんも注意してくださいね。絶対に半透明の液体(それは溶けてるとは言わない、懸濁してるって言うんだ!)なんか打っちゃだめですよ。

